한미약품(대표이사 박재현)이 개발 중인 차세대 비만신약 ‘에페글레나타이드’가 연내 식품의약품안전처 허가 신청을 앞두며, 내년 하반기 국내 출시가 유력시된다. 한국인 대상 데이터 기반으로 한 첫 GLP-1 계열 비만치료제로, ‘국민 비만약’의 탄생 가능성이 커지고 있다.
한미약품은 자사 핵심 R&D 프로젝트 ‘H.O.P(Hanmi Obesity Pipeline)’의 첫 성과물인 에페글레나타이드의 임상 3상 중간 톱라인(topline) 결과를 27일 공시했다. 이번 결과는 투약 40주차 기준으로, 전체 임상 과제는 총 64주차까지 진행될 예정이다.
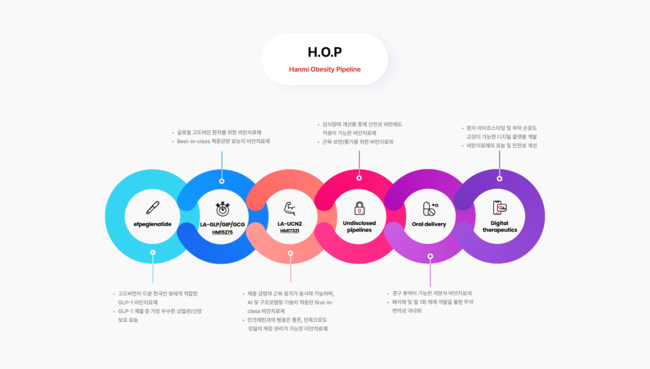 한미약품의 비만혁신 신약 개발 프로젝트인 H.O.P 프로젝트 개요도. [이미지=한미약품]이번 임상에는 한국인 448명이 참여했으며, 투약 40주차 시점에서 시험 대상자의 절반 이상이 체중의 10% 이상을 감량했다. 특히 일부 환자는 최대 30%까지 감량하는 등 높은 효능이 확인됐다.
한미약품의 비만혁신 신약 개발 프로젝트인 H.O.P 프로젝트 개요도. [이미지=한미약품]이번 임상에는 한국인 448명이 참여했으며, 투약 40주차 시점에서 시험 대상자의 절반 이상이 체중의 10% 이상을 감량했다. 특히 일부 환자는 최대 30%까지 감량하는 등 높은 효능이 확인됐다.
또, 구토·오심 등 부작용 비율이 기존 경쟁약 대비 낮게 나타나, ‘효과적이면서 안전한 체중감량’이라는 사회적 요구에 부합하는 결과로 평가받고 있다. 한미약품은 한국인에게 최적화된 GLP-1 계열 비만약으로, 국내 임상 단일 과제로는 가장 많은 데이터를 확보했다고 설명했다.
이번 임상을 주도한 김나영 한미약품 신제품개발본부 전무는 “한국인 임상에서 효과와 안전성을 동시에 입증한 첫 GLP-1 비만신약으로 상용화에 성큼 다가섰다”며 “비만을 넘어 당뇨 등 대사질환 치료 영역으로의 확장 가능성도 열렸다”고 말했다. 한미약품은 이번 중간 결과 발표가 64주차 투약 완료 후의 최종 데이터보다 보수적인 수치일 수 있다고 설명했다. 따라서 연내 허가신청 시점에는 더욱 개선된 지표가 제시될 가능성이 있다.
에페글레나타이드는 인슐린 분비를 촉진하고 식욕을 억제하는 GLP-1(글루카곤 유사 펩타이드-1) 작용제를 기반으로 한 주 1회 투여 제형이다. 미국 일라이릴리의 ‘마운자로’, 노보노디스크의 ‘위고비’ 등과 동일 계열로 분류된다.
한미약품은 "통상 비만약 개발사들이 60주차 이상 투약 결과를 발표하는 것과 달리, 40주차 중간 톱라인 결과를 공개하게 된 건 그만큼 에페글레나타이드의 우수한 경쟁력과 안전성, 시장성을 자신하고 있기 때문”이라며 “연내 허가신청 목표를 차질없이 추진하고, 내년 하반기경 출시될 수 있도록 전사적 노력을 기울일 계획”이라고 밝혔다.
박재현 한미약품 대표이사는 “내년에 출시될 에페글레나타이드는, 한미약품이 또 한번 비상하는 중요한 마일스톤이 될 것”이라며 “에페글레나타이드 출시 이후 순차적으로 선보이게 될 다른 H.O.P 프로젝트의 가시적 성과도 기대되는 만큼, 첫 단추인 에페글레나타이드의 성공적 런칭에 한미의 역량을 더욱 집중시키겠다”고 말했다.
