GC녹십자(대표 허은철)가 자체 개발 치료제를 식품의약품안전처(이하 식약처)로부터 희귀약품 지정을 받으며 미국 FDA, 유럽 EMA에 이어 세 번째 희귀의약품 지위를 획득했다.
GC녹십자는 자체 개발 중인 산필리포증후군 A형(과제명: GC1130A) 치료제가 식약처로부터 희귀의약품 지정을 받았다고 5일 밝혔다.
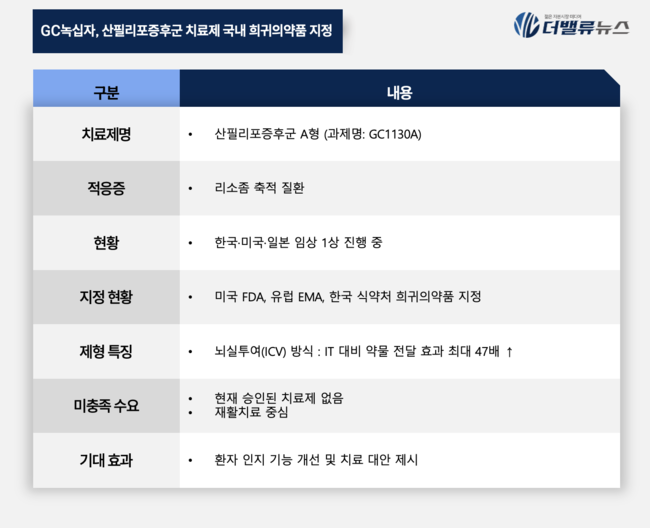 GC녹십자 '산필리포증후군 A형 치료제' 식약처 희귀의약품 지정 주요 내용 요약 도표 [자료=더밸류뉴스]
GC녹십자 '산필리포증후군 A형 치료제' 식약처 희귀의약품 지정 주요 내용 요약 도표 [자료=더밸류뉴스]
국내 희귀의약품 지정은 △유병 인구 2만 명 이하 질환 대상 의약품 △적절한 치료 대안이 없거나 기존 치료제 대비 안전성·유효성이 개선된 의약품에 부여된다. 지정 시 품목허가 신청 전 사전 검토 수수료 감면, 조건부 허가 신청 자격 등 개발 촉진 혜택이 따른다.
산필리포증후군은 리소좀 축적 질환의 일종으로, 소아 약 7만 명당 1명 꼴로 발생한다. 환아들은 2~5세 무렵 언어 발달 지연과 발달 정체를 보이며, 점차 인지 저하·운동 기능 약화·호흡기 합병증으로 이어져 생존에 심각한 위협을 받는다. 현재 승인된 치료제는 없어 재활 치료에만 의존하고 있어 환자들의 미충족 수요가 매우 크다.
GC녹십자는 해당 치료제를 뇌실투여(ICV) 제형으로 개발하고 있다. ICV 방식은 약물을 뇌실에 직접 투여해 뇌 전달 효율을 높인다. 실제로 2024년 발표된 비임상 연구에서 ICV 제형은 척추강 내 직접 투여(IT) 대비 최대 47배 높은 약물 전달 효과를 입증했다. GC1130A는 현재 한국, 미국, 일본에서 임상 1상이 진행 중이며, 5년 내 상용화를 목표로 하고 있다.
허은철 GC녹십자 대표이사는 “국내 희귀의약품 지정으로 개발 속도가 한층 빨라질 것으로 기대한다”며 “GC1130A가 산필리포증후군 환자들의 미충족 의료 수요를 해소할 수 있는 의미 있는 대안이 될 것”이라고 말했다.
