GC녹십자셀(031390)이 식품의약품안전처(식약처)로부터 췌장암 관련 제 3상 임상시험계획(IND)을 21일 승인받았다.
 GC녹십자셀 CI. [이미지=GC녹십자셀 제공]
GC녹십자셀 CI. [이미지=GC녹십자셀 제공]
생물학 제제 제조기업 GC녹십자셀이 기존 간암 항암제 ‘이뮨셀엘씨주’를 췌장암 치료에 사용하겠다고 밝혔다.
지난 7월 신청했던 임상시험계획이 승인됨에 따라 서울대병원 외 14개 임상기관에서 408명의 췌장암 환자를 모집하여 신규 적응증 추가를 위한 상업화 3상 임상시험을 진행할 예정이다.
중앙암등록본부에서 발표한 ‘국가암등록통계’에 따르면 2017년 신규 췌장암은 7032명 발생했으며, 5년 상대 생존율은 12.2%로 최하위를 기록했다.
특히, 모든 암의 5년 상대생존율이 20년 전보다 23.8% 증가한데 반해 췌장암은 1.6% 증가하는데 그쳐, 다른 암종 질병보다 치료 발전이 지지부진한 상황이다.
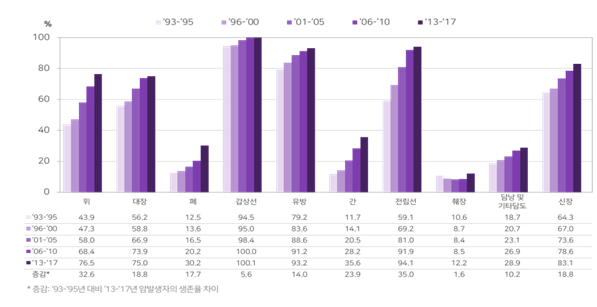 주요 암종 5년 상대생존율 추이. [이미지=GC녹십자셀 제공]
주요 암종 5년 상대생존율 추이. [이미지=GC녹십자셀 제공]
GC녹십자셀에 따르면, 임상시험에 참여하는 환자는 무작위 배정을 통해 젬시타빈 단독치료군과 이뮨셀엘씨주와 젬시타빈 병용치료군으로 나눠 유효성과 안전성을 평가할 계획이다. 차후 암 재발과 사망률 감소를 확인해 이뮨셀엘씨주의 적응증 추가를 진행할 것으로 보인다.
임상시험에 사용될 이뮨셀엘씨주는 환자의 혈액에서 면역세포를 추출하여 특수 배양 과정을 통해 항암능력을 향상시킨 면역세포로 제조 후, 환자에게 다시 주사하는 방식의 항암제다.
이미 2007년 간암에 대한 항암제로 품목허가를 획득했고, 지난해 357억원의 판매실적을 올리는 등 현재 국내 세포치료제 중 매출 1위를 기록하고 있다.
GC녹십자셀 이득주 대표는 "이뮨셀엘씨주의 췌장암에 대한 치료효과는 이미 2014년 말기 췌장암 환자에 대한 연구자 임상시험으로 증거를 확보한 상태"라며 "이번 3상 임상시험을 통해 난치 질환인 췌장암에 대한 치료 옵션을 확보하는데 그 의미가 크다"고 말했다.
